Pham ve ark. (2023) Avustralya, Kanada ve Birleşik Krallık’taki düzenleyici kararlar ve sağlık teknolojisi değerlendirmeleri (HTA’lar) hakkındaki verileri kullanır ve bunları ABD’de FDA onaylı ilaçlarla karşılaştırır. Şunu bulurlar:
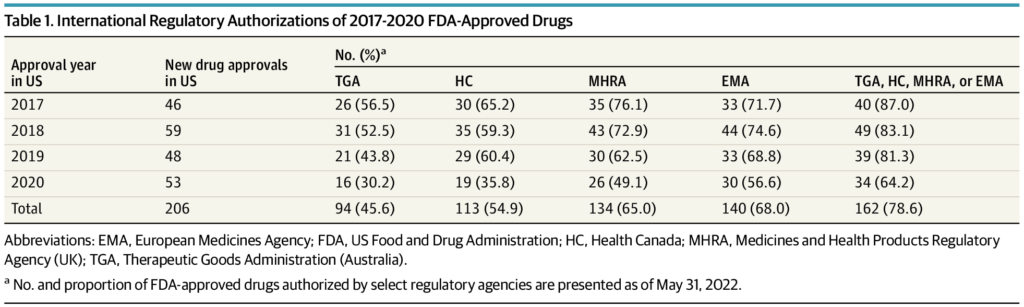
FDA, 2017’den 2020’ye kadar 206 yeni ilacı onayladı ve bunlardan 162’sine (%78,6), ABD onayını takiben medyan (IQR) 12,1 (17,7) aylık bir gecikmeyle en az 1 başka düzenleyici kurum tarafından pazarlama izni verildi. Öte yandan, FDA onaylı 5 ilaca, olumsuz fayda-risk değerlendirmeleri nedeniyle uluslararası bir düzenleyici kurum tarafından pazarlama izni verilmedi. Ek 42 FDA onaylı ilaç, klinik faydaların belirsizliği veya kabul edilemez derecede yüksek fiyatlar nedeniyle Avustralya, Kanada veya Birleşik Krallık’taki STD kurumlarından olumsuz geri ödeme önerileri aldı. Uluslararası bir kuruluş tarafından geri ödeme için onay verilmeyen veya önerilmeyen 47 ilacın ABD’deki medyan (IQR) maliyeti, hasta başına yıllık 115.281 ABD Doları (166.690 ABD Doları) idi. Yirmi ilaç onkoloji endikasyonları içindi ve 36’sı hızlandırılmış düzenleyici yollar veya Yetim İlaç Yasası yoluyla FDA tarafından onaylandı.
Makalenin tamamı Burada.